Raschet - WEGA-project/wega-hpg GitHub Wiki
- Моно-раствор и концентрат
- Монорастворы солей
- Изготовление концентратов A и Б (A and B)
- Как создать свой концентрат микроэлементов и внести его
- Моно-раствор содержит 1 компонент(одну соль) и воду. Определяется концентрацией (г/л) и плотностью (г/мл).
Например моно-раствор Магния Сернокислого(MgSO4) плюс вода.
- Концентрат содержит определенную концентрацию совместимых между собой солей(компонентов), которые не вступают во взаимную реакцию при высокой концентрации, а сохраняются неизменными на всем сроке хранения. Определяется соотношением к рабочему раствору (например '100:1', '200:1'). Это означает что для приготовления 100 или 200 частей, соответственно, рабочего раствора требуется 1 часть концентрата. Как правило, составляют два концентрата, А (концентрат азотнокислых солей) и Б (концентрат сернофосфорных солей).

В данной форме мы можем оперировать жидкими состояниями солей. Для практики это значит раствор делаем не взвешивая каждый компонент, а отмеряя компоненты мерным стаканчиком или шприцем.
Сперва нужно немного поработать, зато потом можно сильно упростить себе жизнь и свести рутину изготовления раствора к минимуму! Например изготовив две бутыли концентрата 200:1 изготовить раствор станет не сложнее чем набрать воды в тару. Пока вода наливается в 10 литровую тару, добавим по 50 мл с бутылок А и B. Получаем 10 литров раствора со скоростью наполнения водой.
- Соли в жидком виде лучше хранятся. Если в сухом виде упаковка не герметична, то многие соли очень активно поглощают воду из воздуха. Этот эффект называется гигроскопичностью. Для нас это значит, что вес хранимого вещества постепенно растет, а само вещество естественно нет, что приводит к нарастанию погрешности взвешивания и несоответствию расчету. И ведь реально вес может вырасти в разы.
- Работа с сухими солями требует использования индивидуальных средств защиты органов дыхания и глаз.
- Сухие соли требуется усердно растворять, тогда как жидкие уже растворены.
- Некоторые соли в сухом виде крайне сложно отмерить, требуются весы высокой точности, тогда как в жидком разведенном виде эта задача резко упрощается за счет большего веса раствора.
- При растворении солей сразу видно их качество, а так-же появляются возможности первичного контроля несоответствия по плотности и электропроводности.
- Ну и соли в жидком виде серьезно экономят время на приготовление рабочего раствора.
- Соли имеют разный предел растворения и в некоторых случаях (например сульфат калия) очень низкий не больше 100 г/л при комнатной температуре. Это означает, что для растворения целой пачки в 1 кг потребуется не менее 10 литров.
- Соли в жидком виде нельзя охлаждать ниже точки кристаллизации. По простому, при разных температурах в воде может быть растворено не более чем определенного количества солей. Это называется точка насыщения раствора. Обычно чем теплее раствор тем эта точка выше и растворить можно значительно больше (в разы). Но стоит температуре упасть, вся "лишняя" соль будет кристаллизоваться на дне. Для нас это значит, что изменится концентрация монораствора и все расчеты с ним потеряют всякий смысл.
Монораствор, это раствор содержащий воду и один компонент, некую одну простую соль. Для монораствора нам важно знать долю вещества, т.е. сколько грамм соли мы внесем добавив столько то миллилитров раствора. Самый простой способ это полное растворение известного веса соли в известном объем тары. Т.е. получение размерность граммы в литре (г/л).
Например изготовим 1.5 литра раствора соли весом 150 грамм.
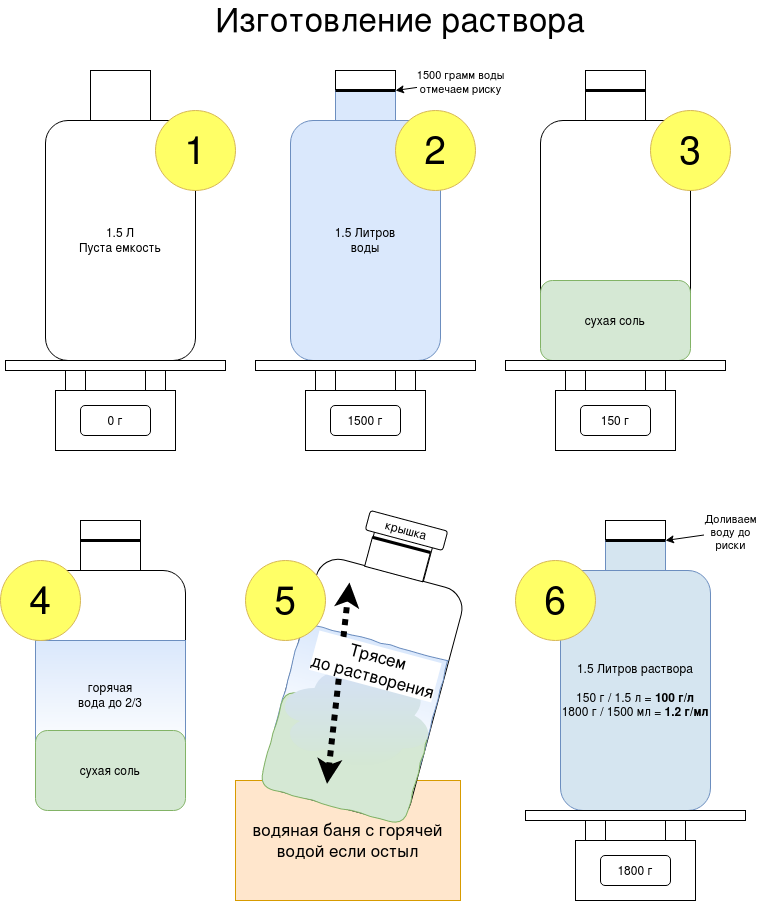
- Тарируем весы с пустой тарой сбрасывая на 0. Если такой функции нет нужно записать вес пустой емкости (сухой) и учитывать его во всех дальнейших расчетах.
- Определяем точный уровень 1.5 литра (тарируем) через вес чистой воды комнатной температуры. Важно использовать тару с сужающимся горлышком, что-бы риска получалась именно на нем. Если нет мерной колбы подойдет бутылка. Известно что вода имеет вес равный 1000 грамм на литр. Т.е. грамм = миллилитру, а значит отмерить объем в случае воды мы можем по весу простыми весами.
строго говоря это не совсем так ведь объем зависит от температуры и примесей, но для нашей задачи этими расхождениями можно пренебречь.
- Засыпаем соль, которую будем растворять. В примере это 150 грамм. То, сколько максимально соли можно засыпать определяем по таблицам растворимости.
- В случае использования бутылки доливаем не больше чем на две трети и плотно закрываем крышкой. Так легче всего растворить соль путем взбалтывания. Растворять желательно в горячей воде, так растворимость всех солей используемых в гидропонике резко возрастает.
- Растворяем до такого состояния, что-бы раствор стал полностью прозрачным. Не допускается наличие осадка в виде недорастворенной соли.
Интересно то, что при растворении соли происходит резкое охлаждение раствора. Это называется эндотермическим процессом растворения кристаллов. Так как при формировании кристаллов (кристаллизации) соли процесс протекал с выделением тепла, то обратный процесс тепло поглощает. Именно по этому может потребоваться подогрев тары с раствором. Для пластиковых бутылок наиболее практична водяная баня. Это емкость с горячей водой. в которую периодически помещается бытылка с раствором. Чем выше температура, тем легче идет процесс растворения.
⚠️ ❗ Нельзя использовать слишком высокую температуру при работе с пластиковыми бутылками. Это может вызвать их деформацию и нарушит тарирование! ❗⚠️
- Доливаем воду до отмеченной в пункте 2 риски. Взвешиваем содержимое. Рассчитываем характеристики для внесения в калькулятор:
Вес сухой соли в граммах делим на объем в литрах 150 грамм / 1.5 литров = 100 г/л.
Это значит что 1 литр раствора будет содержать в себе 100 грамм растворенного вещества, а 1 мл содержит 100 мг вещества. Т.е. 100 г/л = 100 мг/мл = 0.1 г/мл
Значит для получения например эквивалента 5 грамм сухой соли таким раствором нам нужно: 5 г = 5000 мг. 5000 мг / 100 мг/мл = 50 мл
Сколько весит 1 миллилитр в граммах. Делим вес раствора в граммах на объем раствора в миллилитрах.
Например:
1800 гр. / 1500 мл. = 1.2 г/мл
Это значит, что мы можем отмерять жидкости по весу. Допустим нам нужно отмерить 50 мл.
Мы знаем, что 1 мл весит 1.2 г. Делаем расчет.
50 мл * 1.2 г/мл = 60 грамм.
Отмечаем на таре эти значения.
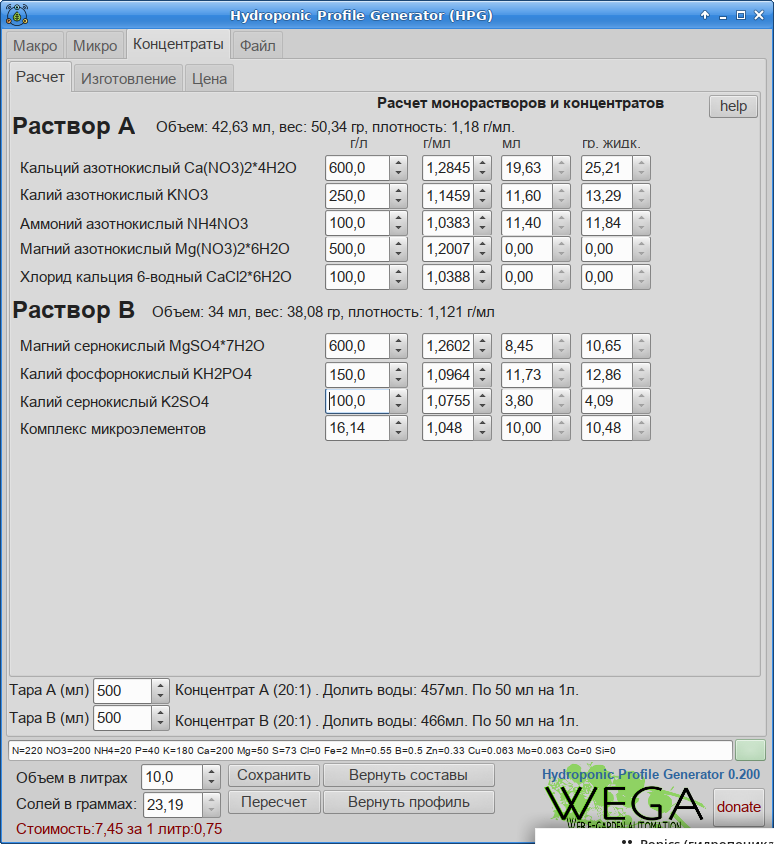
При заполнении поля г/л, будет автоматически проведена попытка определить плотность и заполнить поле г/мл. Плотности определяются по табличным справочным значениям для идеально чистых солей при температуре 20 градусов цельсия (18 для Ca(NO3)2 ) и могут не совпадать с фактическими.
Вносим полученные значения в калькулятор в соотвествующие поля: концентрацию в поле г/л, а плотность в г/мл
Любой гидропонный раствор можно уместить в виде минимум двух концентратов А и Б. Как бы сжать его уменьшив долю воды. Калькулятор позволяет выполнить расчет концентрата. Для этого указываем в поле литры суммарный объем рабочего раствора, который нужно уместить в концентратах, а в полях тара, задаем объем тар для его хранения.
Важно, чтобы подпись долить воды содержала положительное значение. Если это не так, то концентрат с заданной степенью концентрации не может быть создан из указанных выше монорастворов. Для использования концентратов порциями, необходимо обязательно их разбавить водой до заданного уровня в поле тара. Если концентраты делаются как разовая порция (т.е. для заливки целиком сразу) разбавлять водой не обязательно.
✅ В некоторых случаях удобнее сразу делать концентраты сухими солями. Их вес можно посмотреть в соответствующих вкладках расчета профиля для макро и микро элементов.
✅ Примеры концентраций 100:1 это по 100+100 мл каждого концентрата на 10 литров воды. 200:1 это по 50+50 мл на 10 литров воды.
Часто в гидропонике профиль микроэлементов используется один и тот-же для разных растений. Потому удобно создать заранее его в виде отдельного концентрата высокой кратности например 1000:1, а затем уже добавлять комплексно при создании концентратов рабочего раствора.
- Задать нужный микропрофиль во вкладке Микро
- Установить объем 1000 литров для тары в 1 литр
- ВАЖНО: Поставить галочку комплекс по бору
- Растворить все рассчитанные компоненты микроэлементов в выбранной таре
- Во вкладке "Изготовление" в поле г/л для комплекса микроэлементов устанавливаем значение 1000. Теперь можно использовать свой комплекс из расчета 1 мл на 1 литр рабочего раствора и изготавливать концентраты с его включением
По этому я бы настоятельно рекомендовал сделать тестовый замес микрокомплекса и посмотреть на его живучесть. Если выяснится, что соли не растворяются или выпадают в осадок спустя месяц, то нужно будет использовать комплексные микро удобрения в сухом виде или добавлять в концентрат Б или сразу в рабочий бак.
- Задать нужный микропрофиль во вкладке Микро.
- Установить объем 1000 литров для тары в 1 литр и скопировать значение из поля суммы навески солей в граммах например: 16,13520
- Скопировать данные из строки с сотавом, например: Состав: Fe=12,395% Mn=3,409% B=3,099% Zn=2,045% Cu=0,39% Mo=0,39% Co=0% Si=0% 8,06759
- Растворить все рассчитанные компоненты микроэлементов в выбранной таре.
- Переключить калькулятор в режим работы с комплексом микроэлементов и заполнить скопированные ранее значения процентовок
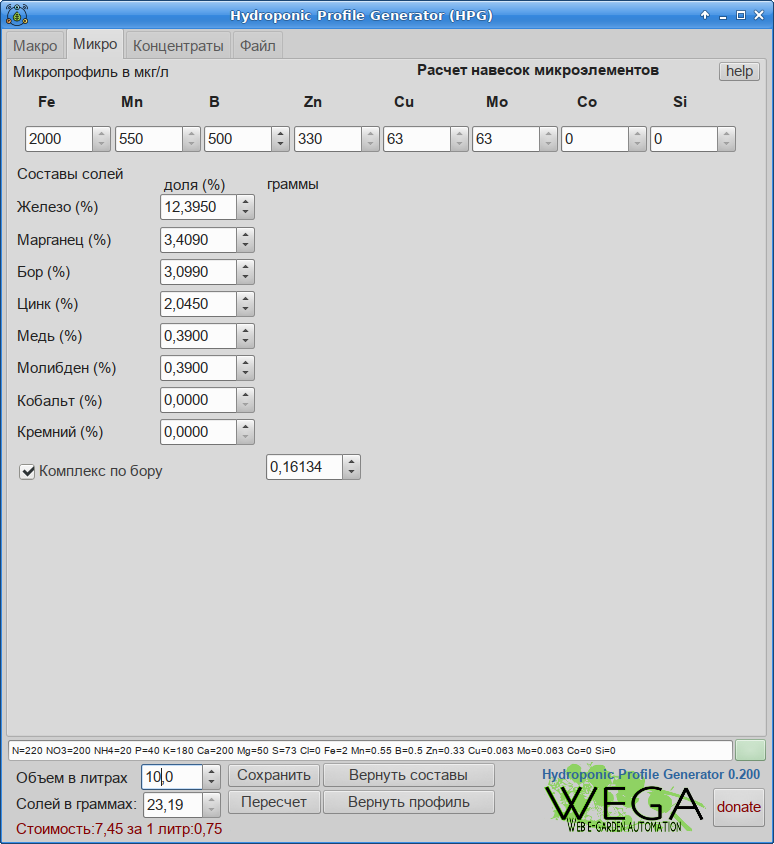
Теперь можно использовать свой комплекс из расчета 1 мл на 1 литр рабочего раствора и изготавливать концентраты с его включением.